ヘパリンと低分子ヘパリン
血液浄化療法で用いられる抗凝固薬として、ヘパリンや低分子ヘパリンがお馴染みですが、違いをきちんと説明できるでしょうか。
今回はこれらの違いを記事にしたいと思います。
ヘパリン(未分画ヘパリン)
ヘパリンは血漿中のアンチトロンビンと結合し活性化することで、抗トロンビン作用により抗凝固作用を発揮します。その他、Ⅹaなどの凝固因子も阻害します。分子量は15000、半減期は40~90分程度です。透析開始時の投与から治療終了にかけての数時間、全身の血液の凝固時間が延長するため、出血病変がある場合、出血を助長する恐れがあります。また、陰性に荷電しているため、陽性に荷電している透析膜や医療材料に吸着されやすいという特徴があります。
低分子ヘパリン
低分子ヘパリンは未分画ヘパリンよりも分子量が小さく4000~6000ほどです。また、未分画ヘパリンよりも糖鎖が短く、アンチトロンビンとは結合できるが、トロンビンとは結合できません。そのため、抗トロンビン作用は未分画ヘパリンのものよりも弱いと言われています。結合したアンチトロンビンは活性化され、Xaなどの凝固因子に結合します。このことから低分子ヘパリンはⅩaを阻害する抗Ⅹa作用により、抗凝固作用を発揮します。抗Ⅹa活性は、体外循環経路内の凝固防止効果が高く、凝固時間延長作用が弱いため、出血傾向のある場合でも、比較的リスクが低いとされています。半減期は2~4時間と未分画ヘパリンよりも長く、陰性に荷電しています。
人工透析と水
透析は大量の"水"を使う医療

「透析」という言葉を聞いて、何を思い浮かべるでしょうか。
「糖尿病」「腎不全」「食事制限」「水分制限」「血液を取り出す」などのイメージをお持ちの方が多く、「水を使う医療」というイメージはないかと思います。血液をきれいにする医療のどの過程に、大量の水が必要なのでしょうか。
今回は、透析で大量の水を使用する理由について簡単に説明したいと思います。
透析って何?
透析で大量の水を使用する理由を説明する前に、「透析とは何か」についてごく簡単に説明したいと思います。
腎臓は、尿の生成やホルモンの産生により恒常性を保っています。透析は、腎臓の機能が不十分な患者さんに対して、腎臓の機能を代替するために行います。しかし、腎臓の機能の全てを代替することはできません。透析では、血液を体外へ導き出し、“ダイアライザ”と呼ばれる膜を通して体内に戻すことで、本来は腎臓で排泄される老廃物や水分を取り除いています。ダイアライザの中では物質交換が起きていて、血液だけでなく水が流れています。
一回(一人)の透析でどれくらいの水が必要か
透析ではダイアライザと呼ばれる膜を使用しますが、このダイアライザの中には血液と水が流れています。この水はダイアライザに1分間に500mℓ(0.5ℓ)供給され、多くの場合、透析は3~5時間施行されるため、一人あたり一回で120~150ℓ必要です。
もし、20人の患者さんの透析を同時に施行するなら、「120~150ℓ × 20人」で、2400~3000ℓの水が必要です。また、透析に使用する水を"透析用水"といい、単なる水道水とは大きく異なっている点があります。
透析液ができるまで

透析液は膜を介して血液と触れるため、ただの水道水を透析用水として使用することはできません。組成も大きく異なっています。どのようにして作られているのでしょうか。
普通の水ではありません
はじめに、透析用水と水道水がどのように違うか説明します。
日本国内の水道水は、厚生労働省の水道法による規定に基づいて、様々な物質の含有量が調整されています。詳細については厚生労働省ホームページをご覧ください。
対して透析液は血液と接するため、表1のようにさらに厳しい基準が設けられています。
表1 透析用水管理基準値(22項目)

(日本臨床工学技士会「透析液清浄化ガイドラインVer.2.01」より)
さらに、生物学的汚染管理基準として、
ET(エンドトキシン)活性値:0.01 EU/mL未満(目標値:0.001 EU/mL未満)
生菌数:1 CFU/mL未満(目標値:0.1 CFU/mL未満)
のように微生物についても規定されています。ちなみに「エンドトキシン」とは、グラム陰性桿菌の細胞壁の構成成分で、血液中に混入すると発熱やショックなどの原因になります。そのため、透析医療に従事するスタッフにとって、エンドトキシンの除去は非常に重要な課題の一つです。
このように、透析用水は厳しい規定に基づいて作製され、透析医療に使用されます。
それではどのようにして透析用水は作られるのでしょうか。
透析用水を作るには?
透析用水が水道水と異なっていることは、お分かりいただけたかと思います。続いて、透析用水がどのような工程を経て作られているのか簡単に解説します。
施設や装置のメーカーによっても異なりますが、透析用水は図1のようなプロセスで作られます。いくつかのフィルタ・装置を通って、ベッドサイドの監視装置に供給されます。図中の各要素にはそれぞれに役割があります。
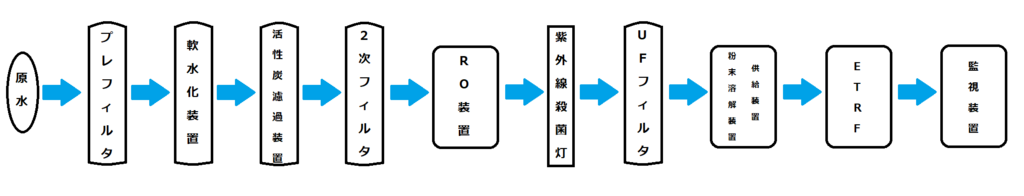
図1 透析用水作製フロー
原水:
原水とは、文字通り透析用水のもとになる水です。水道水を使用している施設が多いですが、地下水を使用している施設もあります。水道水を使用する場合は水道法に準拠していなければなりません。
プレフィルタ:
プレフィルタは原水に含まれる大きな物質を取り除きます。後段の装置・フィルタの目詰まりを防ぐため、水に溶けない細かい物質を除去します。細孔径は25~50μmですので、細孔径よりも小さい物質は膜を通過します。
軟水化装置:
RO膜に沈着する可能性のあるカルシウムやマグネシウムを捕捉する装置です。RO膜はカルシウムやマグネシウムが沈着すると、処理能が大きく低下するため、あらかじめ軟水化装置で取り除いています。
軟水化装置の中にはナトリウムイオンを持つイオン交換樹脂があり、ナトリウムイオンとカルシウムイオン・マグネシウムイオンを交換しています。
活性炭濾過装置:
活性炭が塩素・クロラミンなどを吸着する性質を持っていることを利用してこれらを除去します。
水道水の中では塩素は消毒のために付加されているため、活性炭濾過装置以降の工程では細菌が発生しやすくなってしまいます。
2次フィルタ:
2次フィルタでは、軟水化装置や活性炭濾過装置から生じる微細な物質を取り除きます。孔径は10μm程度でプレフィルタよりも小さくなっています。
RO装置:
ROとは"逆浸透"のことです。RO装置では、加圧ポンプにより1MPa以上に加圧して透過させます。これにより、水に含まれる溶質の99%程度が取り除かれます。
RO装置の処理能力は水温と圧力に比例するため、RO装置に流入する前に原水を加温している施設もあります。
紫外線殺菌灯:
塩素を取り除いた後の水は細菌が繁殖しやすいため、紫外線(波長260nm)によって殺菌しています。
UFフィルタ:
数千~数万程度の分画特性のフィルタで、透析用水作成の最終段です。
この段階では原水は透析用水となっています。
透析用水は、以上のような処理を経て粉末溶解装置や供給装置へ送られます。
透析用水と透析液
見出しでは「透析液ができるまで」としていますが、ここまで「透析用水」という言葉を使っていました。日本臨床工学技士会「透析液清浄化ガイドラインVer.2.01」では以下のように「透析用水」という言葉が使われています。
透析用水は、粉末透析液の溶解や透析液原液の希釈および配管、装置の洗浄・消毒に使用するものとし、原水を濾過・イオン交換・吸着・逆浸透などの方法を用いて処理した後に基準値未満に管理する。
日本臨床工学技士会「透析液清浄化ガイドラインVer.2.01」より
つまり、「透析液」は粉末や原液の透析液を透析用水で希釈して作製されています。図1に示した透析用水作製フローでは、粉末溶解装置や供給装置で希釈・作成が行われています。
透析液には様々な電解質が含まれています。完成した透析液は時間が経つとカルシウム・マグネシウム・炭酸水素ナトリウムが反応して、炭酸カルシウムと炭酸マグネシウムが析出してしまいます。
これらの結晶は透析液の濃度に影響を与えるため、各種の電解質等を「A剤」、重炭酸ナトリウムを「B剤」として分けた形で管理しています。同じ理由から、透析用水とA剤・B剤は供給する直前に混合しています。
A剤・B剤は粉末ではなく液体であることもあります。しかし、粉末タイプは重量・占有スペース・ゴミなどが少ないことから、粉末タイプを使用している施設が多く見受けられます。
希釈された後は、表2のような組成になります。
表2 透析液の組成

これらの電解質やブドウ糖の濃度は、透析液と血液が膜を介して接触した際に重要になります。また、それぞれの値が透析患者さんにとってどのような意味を持つかは、別の記事で紹介したいと思います。
透析液は表2のような組成に調整されてダイアライザへ送られますが、ダイアライザの中では何が起きているのでしょうか。
透析液と血液が出会う場所
さて、ここまで透析用水や透析液の作製工程について説明してきました。
様々な工程を経て作られた透析液は、「ダイアライザ」の中で血液と出会います。ダイアライザは図2のように筒状になっています。
この中には内径200μmのストロー状の膜が3000~15000本程度充填されています。この膜の内側を血液が、外側を透析液がそれぞれ反対向きに流れています。
この膜を利用して、水分や老廃物を除去し、腎臓の代わりをするのがダイアライザです。
それでは、ダイアライザの中では何が起きているのでしょうか。
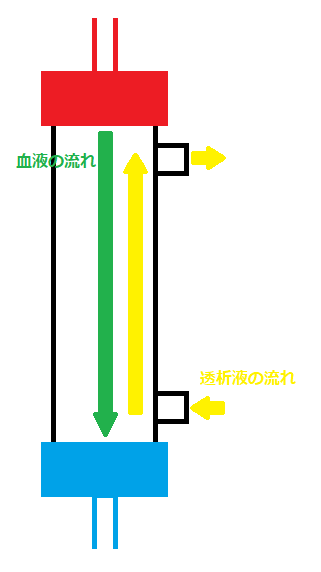
図2 ダイアライザの形状
ダイアライザの中で何が起きているか
最後に、ダイアライザの中で何が起きているかを説明したいと思います。
ダイアライザの中では、「拡散」と「限外濾過」という現象を利用して水分や老廃物を除去しています。
拡散
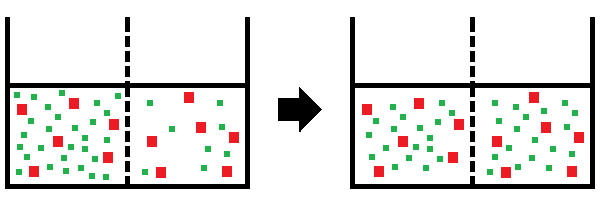
図3 拡散
図3は、溶質が不均一に存在する溶媒を 細孔を持つ膜(半透膜)で隔てた図です。溶質とは液体に溶けている物質、溶媒は溶質が溶け込んでいる液体をいいます。
図3の左側では溶質は不均一な状態です。この時、溶質は濃度の高い方から低い方へ、溶媒は溶質の濃度が低い方から高い方へ移動します。
この溶質の移動を「拡散」、溶媒の移動を「浸透」といいます。これらの現象は濃度差によって引き起こされ、濃度差がなくなると、拡散も浸透も止まります。
透析液の組成はこの濃度差を生むように調整されています。つまり、取り除きたい物質の濃度は血液より低く、補充したい物質の濃度は血液より高く調整しているのです。
細孔よりも大きい物質は膜を通過することができず、一方に留まります。
透析では、この現象を利用して老廃物の除去を行っています。また、血液中に含まれる物質の中でも、体に必要なもの(血漿タンパクなど)は極力通過しないように膜が設計されています。
限外濾過
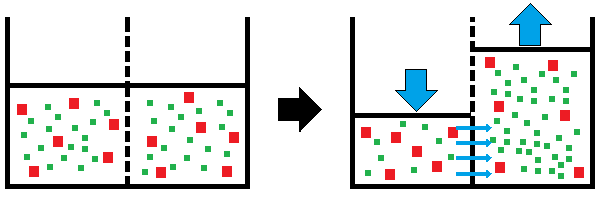
図4 限外濾過
図4では均一な溶液を半透膜で隔て、一方に圧力をかけています。すると、膜の細孔よりも小さい物質と液体成分がもう一方へ移動します。このような現象を「濾過」といい、膜の平均細孔径を分子のサイズ(1nm)に近づけた濾過を特に「限外濾過」といいます。
限外濾過では溶質の移動は、圧力によって起こります。
透析では、この現象を利用して血液中の水分を透析液に移すことで取り除いています。細孔よりも小さい溶質成分を除去することもできるため、併せて透析の重要な原理なっています。
まとめ
「透析液がどのように作られているか」や「ダイアライザの中で何が起きているか」について、患者さんに易しく説明することは意外に難しかったりします。
今回は、最近透析業務から離れることの多い自分が、基礎的な知識を思い出すために記事を書きました。
一般的な消毒薬
各種消毒薬はそれぞれ固有の抗微生物スペクトルをもつことから、消毒薬を使用する上で留意して選択しなければ、期待する効果を得られない。
病原微生物の分類
微生物の大きさは、寄生虫、真菌、細菌、リケッチャ、クラミジア、ウィルス、プリオンの順に小さくなる。原虫の一部や真菌、細菌の細胞は、赤血球よりも小さく、通常は数十μm程度である。頻繁に名前を目にする微生物の中でも、エキノコックス、マラリア、ニューモチスカリニなどは原虫、カンジダ、クリプトコッカス、水虫などは真菌である。これらは、真核生物と呼ばれ、核膜で囲まれた核を持つ細胞からなり、細胞分裂時に染色体構造を生じる生物である。細菌、リケッチャ、クラミジアは原核生物
と呼ばれる。原核生物とは核膜のない細胞からなる生物である。
細菌とウィルス
細菌の細胞の外側には細胞壁があり、多糖類とペプチドから構成されている。細胞の中にはタンパク質合成を行うリボソームや、細胞呼吸を司るメソソームなどが存在する。原核生物である細菌は明確に区別できる核を持たないが、遺伝情報を司るDNAは糸状に集塊を作って、細胞内に存在する。大きさは、通常0.5~10μm程度である。
対してウィルスはタンパク質の外殻の内部にDNA、もしくはRNAを持っただけの微生物であり、細菌のように栄養を摂取してエネルギーを生産するような生命活動を行わない。ウィルスは細胞をを宿主とするため、大きさは0.02~0.45μmと、細菌に比べ小さい。また自身で増殖する能力はなく、他の生物を宿主にして自己を複製することでのみ増殖する。
人体・環境・器具に使用する消毒薬
塩化ベンザルコニウム・塩化ベンゼトニウム
第4級アンモニウム塩で、陽イオンを持つ原子団が菌体表面の陰イオン部分に吸着し、細胞内に浸透して細胞膜の構造を破壊する。
陽イオン界面活性剤(逆性石鹸)であり、消毒効果と界面活性作用による洗浄効果を有する。石鹸などの陰イオン界面活性剤との混合により効力が低下する。皮革製品や合成ゴム、合成樹脂、光学器具、鏡器具、塗装カテーテルには使用しない。一般細菌や感受性緑膿菌や梅毒トレポネーマには有効であるが、ウィルスには効果がない。皮膚や創傷面、粘膜の消毒に使用できるほか、金属と非金属の消毒にも使用できる。
グルコン酸クロルヘキシジン
陽イオンを持つことから菌体表面の陰イオン部分に吸着し、比較的低濃度で細菌の細胞膜に障害を与え、細胞質成分の不可逆的な漏出や酵素阻害を起こし静菌的に作用する。0.01%以上の比較的高濃度では細胞内の蛋白や核酸の沈着を起こし殺菌作用を現わす。
グルコン酸クロルヘキシジンは低毒性であることから、創傷部位や手洗い時、手術野の消毒に繁用される。しかし、膣や膀胱などの粘膜面への使用ではショックの報告があり、脳、脊髄、耳への使用では、難聴や視覚障害を起こすことがあるため禁忌である。金属器具の長時間の浸漬時には防錆剤の亜硝酸ナトリウムを添加する。塩化ベンザルコニウムと同様に、石鹸との混合により効力が低下する。一般細菌と感受性緑膿菌、梅毒トレポネーマに対しては有効であるが、ウィルスには効果が認められていない。皮膚や創傷面、金属、非金属に対して消毒を行うことができるが、粘膜に対しては、上述の理由から使用は禁忌である。
消毒用エタノール・イソプロパノール
細菌の細胞膜中の脂質を溶解し、タンパク変性を惹起する。また、アルコールの脱水作用により、細胞内に浸透すると液体成分とともに蒸発させるため、細胞内部を乾燥させることで殺菌作用を現わす。
抗菌スペクトルが広く短時間で効力を発揮することから広範囲に使用できる。さらに、他の消毒薬との混合使用で効果を高めるが、上述のような脱脂作用があり、頻回の皮膚への使用は適さない。粘膜や創傷面に対しても刺激があるため用いない。器具に対しては金属・非金属ともに変質することがあるため適さないが、一般細菌、MRSA、緑膿菌、梅毒トレポネーマ、結核菌、真菌に対して有効である他、エンベロープを持つウィルスやエイズに対しても効果を発揮する。
人体に使用する消毒薬
ポピドンヨード・ヨウ素
ヨウ素の酸化作用により菌体タンパク中の-SH基、=NH基、-OH基などを酸化、破壊して細胞内のタンパクを変質させて殺菌作用を示す。殺菌力は中性からアルカリ性で強く現れる。
ポピドンヨードはヨウ素にキャリアであるポリビニルピロリドンが結合した水溶性複合体で、徐々にヨウ素を放出するため毒性が低く、人体に広範囲で用いられるが、金属腐食性が強く、皮膚や衣類などを着色する。石鹸などの陰イオン界面活性剤との併用により効力が低下する。ヨウ素においてもポピドンヨードと同様の殺菌作用や作用機序であるが、皮膚刺激が強いため、使用は減少している。また人体への使用においては、長時間・広範囲の使用の際に血中ヨウ素濃度上昇の可能性があり、ヨウ素過敏症に注意する。細菌芽胞とB型肝炎ウィルス、C型肝炎ウィルス以外の微生物に対して有効であるが着色や強い腐食性のため、器具や環境の消毒には使用しない。
オキシドール
血液や体組織に含まれるカタラーゼにより分解して発生期の酸素を放出し、強力な酸化作用により殺菌作用を示す。漂白作用、脱臭作用も有する。
殺菌作用と、発生する大量の酸素の泡が洗浄効果を有し、汚れた外傷に繁用される。浸透性が弱く、持続力も短いため、低濃度、短時間での殺菌作用は弱い。低毒性、低刺激性であるが、発癌性の報告がある。抗菌スペクトルは狭く、一般細菌にのみ効力が認められている。
環境に使用する消毒薬
次亜塩素酸ナトリウム
水と接触して次亜塩素酸(HOCl)または塩素ガスを生成し、主に次亜塩素酸の作用により殺菌作用を示す。細菌の細胞膜に浸透して酵素タンパク、核タンパクの-SH基を分解して殺菌作用を示す。また、ウィルスの構成タンパクなどを酸化して不活性化する。
強力な消毒薬であり、漂白作用、脱臭作用も有する。濃度0.1%以上では強アルカリ性で刺激が強い。金属腐食作用が強く、多くの材料を変質させることがあるため、長時間の浸漬は適切ではない。酸性の洗浄剤との混合では大量の塩素ガスが発生するため併用は禁忌である。抗菌スペクトルは広く、エンベロープを持つウィルスやB型肝炎ウィルス、C型肝炎ウィルスにも適応するが、細菌芽胞と結核菌に対しては有効ではない。
グルタラール(グルタルアルデヒド)
分子中のアルデヒド基(-CHO)が、菌体タンパク中の活性基(-NH2、=NH、-SH)などと反応してタンパク合成阻害などにより殺菌作用を示す。アルカリ性では反応が速くなる。
現存する消毒薬の中では最も強い殺菌力を持ち、種々の材質の消毒に適する。さらに、B型肝炎ウィルス、C型肝炎ウィルスを殺菌できる上、エンベロープを持つウィルスや細菌芽胞に対しても有効である。有機物の影響を受けにくいが、器具や環境の消毒においては、付着している体液等の汚れは予備洗浄して用いる。蛋白凝固作用を有するので、人体への使用は不適である。眼や呼吸器系の粘膜刺激、皮膚炎や皮膚の白色化、硬化などが生じるため、付着や吸入に注意する。消毒に使用する際は、通気性の良い場所でプラスチックエプロンやゴム手袋を着用して取り扱う。
クレゾール石鹸液
タンパクと緩く結合しタンパク変性を起こす。高濃度では細菌タンパクを凝固させ、低濃度では細胞壁に作用して溶菌させる。また、細胞膜に対する浸透性が強く、細胞膜の機能低下・破壊を起こし、細胞質のタンパクと結合して酵素作用を不活性化し細菌を死滅させる。
腐食性で皮膚刺激が強く、損傷皮膚から吸収されやすいため、人体への使用は不適である。殺菌作用と石鹸の洗浄効果を併せ持ち、有機物の影響を受けにくく、有機物への浸透性が良いので、糞便・喀痰や環境の消毒に用いられる。皮膚や衣類等に対しては着色があるため使用しない。
血液凝固系・RAA系・KK系
血液透析においては血液が回路やダイアライザなどの異物と接触し、血液凝固反応が惹起され、凝血のため体外循環は中断される場合がある。RAA系は 様々な病態において機能の低下が認められるが、透析患者に多いとされる糖尿病もその病態の一つである。また、血液凝固反応が起きると、同時にKK系の反応が進み、血圧のコントロールに影響を与える。このことから、これら3つの生体反応について知識を持つべきであると考える。
血液凝固系
血液凝固に関わる物質を血液凝固因子と呼ぶが、これらは生理的状態では不活性な形で血中を流れている。血液凝固因子は第Ⅰ因子であるフィブリンから第XⅢ因子まであり、いずれも蛋白質で一部が切断されると活性を持った酵素となり、下位の凝固因子を活性化する。
血管内皮が傷害され、血液が血管内皮下の組織に接触すると、血液凝固の為に第Ⅻ因子が活性化され、活性化第Ⅻ因子となり、内因系血液凝固が起こる。第Ⅻ因子は内皮細胞以外の陰性荷電物質と接触することで活性化することが知られている。
外因系血液凝固は血管内皮細胞の損傷程度では起こらず、組織が破綻し、組織中の組織因子である第Ⅲ因子やトロンボプラスチンが露出したときに活性化される。これら2つの凝固反応は、終段では可溶性のフィブリノゲンがトロンビンの作用で不溶性のフィブリンとなって凝固する。
RAA系
RAA(レニン-アンギオテンシン-アルドステロン)系は生体内において血圧と体液量の調整機構として重要な役割を演じている。RAA系は、尿中NaCl濃度の低下、腎血流量の減少、ノルアドレナリンの放出などによって惹起される。
腎臓の輸入細動脈の壁にある傍糸球体細胞からレニンが分泌され血液中のアンギテンシノーゲンからアンギオテンシンⅠが産生される。アンギオテンシンⅠはアンギオテンシン変換酵素(ACE)によりアンギオテンシンⅡに変換される。アンギオテンシンⅡは全身の動脈を収縮させるほか、副腎皮質からのアルドステロンの生成・分泌促進作用を持つ。これらの作用を有することから、ACE阻害薬やアンギオテンシンⅡ受容体拮抗薬は高血圧治療薬として用いられる。この結果産生・放出されたアルドステロンは、Naを体内に溜める働きがあり、これにより循環血液量が増加して心拍出量と末梢血管抵抗が増加することで血圧を上昇させる。アンギオテンシノーゲンは血管、腎臓、脳、副腎、肝臓、卵巣など生体内で広く生産されている。また、レニンは血圧上昇後に分泌が低下し、RAA系の働きが低下する。
腎血管性高血圧では、腎血管の狭窄などによる腎血流量の減少に伴い、糸球体濾過量が減少することで、緻密斑に到達するNaCl濃度が低下することでレニンの分泌が亢進するため、RAA系もその働きを増す。
KK系
KK(キニン-カリクレイン)系は血管内皮の損傷により、血液凝固系で活性化された活性化第Ⅻ因子はKK系においてプレカリクレインをカリクレインに変換することで反応が進む。カリクレインはタンパク分解酵素であり、キニノゲンに働いてブラジキニンというポリペプチドを産生する。ブラジキニンは発痛物質である他、血管拡張作用や血管透過性亢進作用を有する。さらに、集合管に作用して尿中へのNaの排泄を増加させ、血圧を低下させる作用を持つ。ブラジキニンは、KK系の最終段においてホスホリパーゼA2を活性化させ、アラキドン酸をPGE2に変換する。PGE2にも弱い発痛作用や血管透過性亢進作用、血管拡張作用を有するが、PGE2はブラジキニンの発痛作用を増強し、痛覚過敏にする。
アンギオテンシン変換酵素はRAA系ではアンギオテンシンⅠに作用し血圧上昇を招くが、KK系ではブラジキニンと拮抗することで不活性化し、血圧の低下を抑制する。カリクレインはブラジキニンの産生に関与する他、第Ⅻ因子の活性化を促進することで、内因系血液凝固反応の引き金にもなり得る。
B型肝炎ウィルスとC型肝炎ウィルス
B型肝炎ウィルスとC型肝炎ウィルスは、肝炎の主な原因として知られています。これらによる肝炎はウィルス性肝炎と呼ばれ、肝硬変や肝癌につながることもあるため、適切な治療を行う必要があります。
肝炎ウィルスにはA~Eの型がありますが、ここでは血液や体液を介して感染し、医療現場で見かけることの多い「B型肝炎」と「C型肝炎」について記します。
B型肝炎
B型肝炎ウィルスはDNAウィルスに属しています。外被にはHBs抗原、芯の部分にはHBc抗原とHBe抗原を持っています。そのさらに内側にDNAが存在しています。また、外被タンパクの組み合わせから、「adw」「adr」「ayw」「ayr」の4つの「サブタイプ」に分けられます。
HBs抗体とはHBs抗原に対する抗体で、過去にB型肝炎ウィルスに感染していたか、ワクチンを接種した後に陽性となります。血液検査で「HBs抗原陽性」とはB型肝炎ウィルスに感染していることを意味します。HBs抗体は「中和抗体」と呼ばれ、抗原に結合して抗原の活性を消失させる働きがあります。しかし、サブタイプが異なるB型肝炎ウィルスの感染では、HBs抗原とHBs抗体が両方とも陽性である場合があります。
HBc抗原はB型肝炎ウィルスを構成するタンパク質で外被の内側に存在します。そのため、検出が難しく日常的な検査が難しいとされています。HBc抗体が低値であるときは、過去にB型肝炎ウィルスに感染していたことを示します。高抗体価の場合は現在B型肝炎ウィルスに感染していることを示し、ほとんどはHBs抗原も陽性です。
B型肝炎ウィルス感染初期に出現し、2~12か月に陰性化するマーカーとして「IgM型HBc抗体」があります。高抗体価陽性ではB型急性肝炎、低抗体価陽性ではB型慢性肝炎の急性増悪やB型急性肝炎を意味します。たとえHBs抗原が陰性である場合でもIgM型HBc抗体が陽性であればB型急性肝炎が疑われます。
HBe抗原はB型肝炎ウィルスの増殖時に産生される可溶性タンパクです。陽性であるときは血液中のB型肝炎ウィルスの量が多く感染性が強いことを意味します。HBe抗体はウィルスの増殖が減退し、HBe抗原産生がHBe抗体量を下回るとHBe抗体が検出されます。HBe抗体が陽性の場合、ウィルスは存在するが量は少なく、慢性肝炎では活動性・感染性は低いことが多いとされています。
感染経路
B型肝炎ウィルスは血液や体液を介して感染し、多くは母子感染によるものです。出産の際に産道で血液を介して、生まれる子供が感染してしまいます。しかし、国内ではワクチン接種が一般的となっており、垂直感染の数は減少しています。また、性的接触による感染も考えられます。
C型肝炎
C型肝炎ウィルスはB型肝炎ウィルスとは異なり、RNAウィルスです。さらに、エンベロープを持っています。血液を介して感染し、急性肝炎を呈することが多く、60~70%は慢性化し、肝硬変や肝癌へ移行することがあります。
HCV抗体はC型肝炎ウィルスに感染すると血液中に現れ、発症2週間以降に陽性化しますが、ときには6か月後に陽性となることもあります。抗体価が低いときには過去の感染、高いときには現在の感染を示していますが、中間的な値では過去の感染と現在の感染の両方が考えられます。
そのため、HCV-RNA検査により両者を鑑別します。HCV-RNA検査はHCVのウィルス量を調べる検査で、PCR法と呼ばれる方法が用いられます。C型肝炎の進行に伴いHCV-RNAの値が高値になります。
原因
B型肝炎ウィルスと同様に血液を介して感染し、空気感染や経口感染はしません。国内では、注射針の使いまわしや医療機関での針刺し事故、古い時代の血液製剤使用、入れ墨、ピアスなどで感染するとされています。C型肝炎ウィルスでは、性的接触や垂直感染は少ないとされています。
抗血小板薬
血栓は脳梗塞や心筋梗塞の原因となるため予防が必要です。予防のためには血栓形成を防ぐ薬を服用します。血栓の形成は、血管が傷つくことで始まります。血管が損傷すると血小板の粘着性が高まると同時に血小板内で「トロンボキサンA2」の産生が亢進します。さらにトロンボキサンA2は血液中に放出され、「セロトニン」の作用により血小板が凝集を始めます。
また、凝固因子の活性化によりタンパク質の一つである「フィブリン」が産生されます。そして活性化された血小板がフィブリンや赤血球とともに血栓を形成します。
本来であれば、出血を止めるための機構ですが、個人の体質、血栓の性質や形成される場所によっては大事に至ることがあります。そのため、抗血小板薬や抗凝固薬の服用により予防する必要があります。
抗血小板薬
アスピリン
トロンボプラスチンA2は血小板内でプロスタグランジンから作られますが、少量のアスピリンを投与すると、シクロオキシナーゼの抑制を介してプロスタグランジンの産生が抑制されます。その結果、トロンボキサンA2が減少し血栓形成が抑制されます。
しかし、アスピリンは大量に投与するとプロスタグランジンの一つであるプロスタサイクリンの産生が抑制されます。プロスタサイクリンは血小板凝集を抑制する働きがあります。そのため、アスピリンの大量投与では血小板凝集が生じ、血栓ができやすくなってしまいます。(アスピリンジレンマ)
オザグレルナトリウム(トロンボキサン合成酵素阻害薬)
オザグレルナトリウムはトロンボキサンA2を作る際に必要なトロンボキサン合成酵素の働きを妨げ、プロスタグランジンからトロンボキサンA2の産生を抑えることで抗血小板薬として効果を発揮します。
トロンボキサンA2に変換されなかったプロスタグランジンはプロスタサイクリンの材料となり血小板凝集抑制作用を示します。
オザグレルナトリウムはトロンボキサンA2の産生抑制に加え、プロスタサイクリンの作用により血栓形成を抑制します。
製剤例・・・オザグレン オザグレルNa キサンボン カタクロット ベガ ドメナン など
チクロピジン塩酸塩・クロピドグレル硫酸塩・プラスグレル塩酸塩(ADP受容体拮抗薬)
血小板が活性化されるとATPやADP、Caイオン、セロトニンが放出され、これらは血小板凝集を促進します。ADP受容体拮抗薬は、血小板膜上の「アデノシン二リン酸(ADP)」受容体を阻害することで血小板の活性化・凝集を抑制します。
また、cAMPの濃度上昇によりトロンボキサンA2の産生を抑えるとも考えられています。
製剤例(チクロピジン塩酸塩)・・・パナルジン
製剤例(クロピドグレル硫酸塩)・・・プラビックス
製剤例(プラスグレル塩酸塩)・・・エフィエント
サルポグレラート塩酸塩
血小板は活性化すると、血液中にセロトニンを放出して他の血小板を活性化させます。サルポグレラート塩酸塩はセロトニン受容体を遮断して、血小板凝集を抑えます。
製剤例・・・アンプラーグ サルポグレラート塩酸塩 など
糖尿病治療薬の種類
スルホニルウレア(SU)系
スルホニルウレア系薬は、膵臓のランゲルハンス島β細胞に存在するSU受容体に作用し、カルシウムイオンを増加させインスリンの分泌を促進する。
さらに、筋肉のブドウ糖を取り込む力を向上する作用や肝臓からのブドウ糖の放出を抑える作用をもつ。
製剤例・・・アマリール オイグルコン ダオニール グリミクロン など
ピグアナイド(BG)系
私たちの体内では、肝臓でグリコーゲンが分解されてブドウ糖になる糖新生がという現象が起きている。ピグアナイド系薬は糖新生を抑え、糖が腸から吸収されにくくしインスリンの反応性を向上させる作用を持つ。
製剤例・・・メトグルコ メデット メルビン グリコラン ジベトス など
インスリン抵抗性改善薬
インスリンが十分に分泌されているにも関わらず血糖値が異常高値を示す場合にはインスリン抵抗性が亢進していることが疑われる。この原因としてTNF-αというサイトカインの増加が挙げられる。TNF-αはPPAR2と呼ばれる、脂肪細胞の分化を促進する物質の働きを弱めるとされている。インスリン抵抗性改善薬はTNF-αの働きを抑え、PPAR2の活性を高めることで、インスリンの反応性を改善すると考えられている。
製剤例・・・アクトス アメル ピオグリタゾン錠「~」 など
αグルコシターゼ阻害薬
食物中の糖は唾液によって二糖類に分解され、腸に存在しているαグルコシターゼという酵素によりブドウ糖に分解・吸収される。αグルコシターゼ阻害薬は、二糖類に似た構造をとっているため、αグルコシターゼと結びつき、本物の二糖類と反応しにくくする働きを持つ。その結果、ブドウ糖に分解されるまでに時間がかかり、糖の吸収が穏やかになるため、急峻な血糖値の上昇を抑えることができる。
製剤例・・・ベイスン セイブル グルコバイ など
アルドース還元酵素阻害薬
糖尿病が進行するとグルコースの処理がうまくいかず、ソルビトールとして蓄積される。ソルビトールが神経細胞に蓄積すると、細胞の機能低下や血流低下などにより神経組織に障害を与える。
アルドース還元酵素阻害薬は、グルコースがソルビトールに変換される過程で働くアルドース還元酵素の働きを阻害し、ソルビトールの生成を抑える。
製剤例・・・キネダック エパルレスタット など
DPP-4阻害薬
食事を摂取すると消化管からインクレチンというホルモンが分泌され、インスリンの分泌を促進する。インクレチンはグルカゴンの放出を抑制するが、血糖値が80mg/dlを下回るとインスリン分泌促進作用とグルカゴン放出抑制作用を停止する。そのため、インクレチンの分泌により低血糖を起こすことは少ないと言える。
インクレチンは食事の摂取後に分泌されても、DPP-4(ジペプチジルペプチターゼ)により分解されてしまい、インスリンの分泌を促進する作用は期待外れなものとなる。DPP-4阻害薬はインクレチンの分解を抑え、作用を持続させることで血糖値の上昇を抑える。
製剤例・・・エクア ネシーナ トラゼンタ オングリザ テネリア ジャヌビア スイニー など
GLP-1アナログ製剤
インクレチンの中でもGLP-1(グルカゴン様ペプチド-1)を注射で補い、GLP-1受容体を刺激してインスリンの分泌を促進する。本来、GLP-1はすぐに分解されてしまうがGLP-1アナログ製剤はGLP-1が長時間持続するように構造を改良している。
製剤例・・・トルリシティ ビクトーザ ビデュリオン バイエッタ リキスミア など
SGLT2阻害薬
糖は腎臓(近位尿細管)から再吸収されるが、過剰となると再吸収されず尿へ排出され「尿糖」となる。糖が再吸収される際にはSGLT(ナトリウム・グルコース共輸送担体)という物質が関与する。SGLTには1と2が存在しているが、糖の再吸収に積極的に関わるのはSGLT2である。SGLT2阻害薬はSGLTを阻害し、糖の再吸収を抑え尿中に糖を排出することで血糖値を下げる作用を持つ薬である。
製剤例・・・ジャディアンス カナグル フォシーガ デベルザ アプルウェイ ルセフィ スーグラ など